بحث عن نظرية الكم والذرة التي درسها الكيميائيون ، في خلال القرن العشرين للتعرف على مستويات الطاقة ، و تفسير سلوك الذرة ، حيث كانت البداية بإكتشاف ، الالكترونات في سنة 1897 ميلادية ، و في هذا الوقت إكتشف العالم طومسون ، تواجد العديد من الجزئيات الرئيسية ، تتواجد في الذرات ، ثم بعد مرور 14 عاما أظهر العالم رذرفورد ، وجود أغلب الكتلة الخاصة بالذرة ، تتواجد داخل نواة صغيرة الحجم ، و يصل نصف قطر النواة 100000 مرة ، من الكتلة الموجودة بالذرة .
بحث عن نظرية الكم والذرة

نظرية الكم عبارة عن جزء هام من الفيزياء الحديثة ، و تقوم هذه النظرية بالإهتمام بالدراسة ، للسلوكيات الخاصة بالمادة و الضوء ، في المستويات الذرية و الغير ذرية ، أي على مقياس الأبعاد بالنانومتر ، و ذلك لأن النانومتر الفردي يعادل 1×10-9 متر ، و تقوم نظرية الكم بعدة محاولات ، لتفسير السلوكيات الخاصة بالذرة ، و محتوياتها الرئيسية .
سلوك الذرة مثل الالكترونات ، و النيوترونات ، و البروتونات .
المكونات الرئيسية للذرة صغيرة الحجم ، عبارة عن الكواركات المتجمعة ، أو المنفردة بكل واحدة على حدة .
إقرأ أيضا
نظرية الكم
في السنوات التي تتراوح بين عام 1858 ميلادية ، حتى عام 1947 ميلادية ، وضع العالم ماكس بلانك نظرية الكم ، التي كان محتواها أن الأشعة الموجودة بالضوء ، تم صنعها من بعض الفوتونات التي تتكافأ ، مع جزئيات حركة الموجة ، مما أدت هذه الاكتشافات ، إلى إنتاج العديد من المفاهيم الحديثة ، و حين تم إدماج النظريات و الاكتشافات ، و المفاهيم الحديثة هذه مع بعضها البعض ، تم ظهور العديد من الأفكار المستجدة ، مما أطلق عليها نظرية الكم ، و في معظم الأحوال يشار إليها بميكانيكا الكم ، و سميت بهذا الاسم نظرا ، للطبيعة الغير متصلة لمستويات الطاقة المختلفة ، في النظم المجهرية التي توفر الكثير من التفسيرات القوية و الجيدة ، من ظواهر العالم الذرية و الشبه ذرية .
إقرأ أيضا
تعريف الذرة
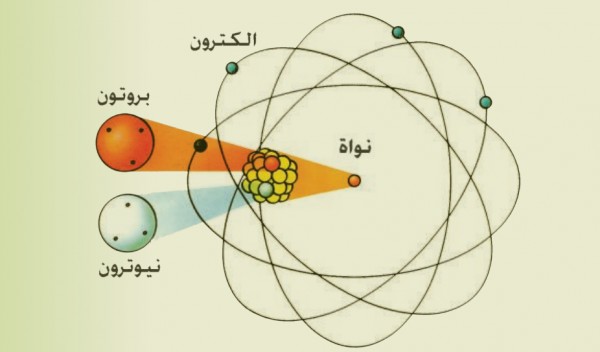
الذرة عبارة عن أساسيات تقوم ببناء الكون و تكوينه ، و هي تحتوي على النيوترونات ، و البروتونات الموجودة في النواة ، التي يلتف حولها الالكترونات المدارية .
نموذج العالم بور لذرة الهيدروجين
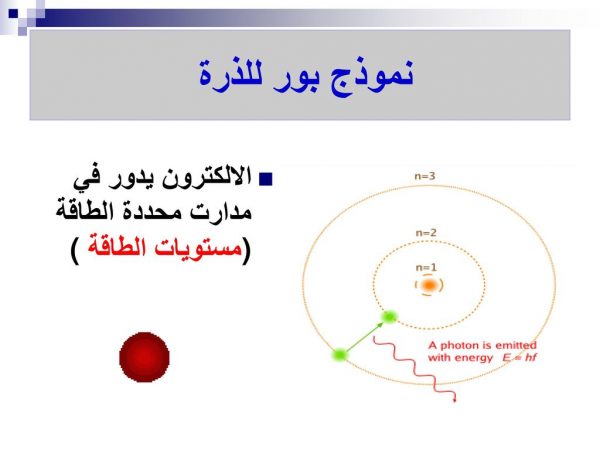
من أبسط الأمثلة على الذرة ، نموذج العالم بور لذرة الهيدروجين ، و هو يعتبر أول نموذج مختلف و غير تقليدي عن الذرة ، من خلال توضيح أطياف الإنبعاث لمختلف العناصر ، التي تتكون من خطوط منفصلة ، ثم يتم ظهور هذه الخطوط على هيئة أربعة أطوال موجية ، يتم إنبعاثها من خلال الضوء في المنطقة المرئية ، و ينبعث منها أطياف الانبعاث لذرة الهيدروجين ، من خلال خطوط يتم تشكيلها من أربعة أطوال ، تصل إلى 410 ، و 434 ، و 486 ، و 656 نانومتر ، و يعبر هذا الانبعاث الكمي عن وجود الالكترونات ، التي لا يثبت وجودها ربما إلا في داخل الذرة ، عند بعض الطاقات الذرية و الأقطار ، و من خلال هذا النموذج قام العام بور بإستخراج ، معادلة المستويات المختلفة للطاقة في ذرة الهيدروجين ، و ساعد ذلك النموذج في نجاح التنبوءات ، الخاصة بمستويات الطاقة المختلفة ، في الأنظمة الأخرى التي تتكون ، من إلكترون واحد مثل الهيليوم .
إقرأ أيضا
الضوء و المادة
أثبت العالم ماكس بلانك و العالم الفيزيائي ألبرت أينشتاين ، في نظرية الكم و الذرة ، أن يمكن للضوء و المادة أن يتم ظهورهم ، كموجات و جسيمات ، حيث إذا كانت هذه الجسيمات متشابهة مع الالكترونات ، يتم ظهورها كموجات ، و يشير هذا إلى أنها لا تمتلك موقع دقيق ، و واضح بالنسبة للجسيم .
