امثلة على تفاعلات ماصة وطاردة للحرارة وتعد الحرارة مصدر هام وقوى على كوكب الارض ونحصل عليه من الشمس كمصدر أول وطبيعى وبعد التطور الهائل فى العلم وتقدمه أصبح هناك تفاعلات كيميائية تساعدنا فى الحصول على الحرارة بحيث تكون الحرارة صور من صور متعدده ناتجة عن الطاقة الناتجة لهذه التفاعلات فقد تصدر على هيئة ضوء أو صوت ايضاً وتعد التفاعلات الباعثة للحرارة تحدث بشكل تلقائى وهى موضوع حديثنا اليوم,
أهم امثلة على تفاعلات ماصة وطاردة للحرارة

- ويوجد نوعين من التفاعلات الكيميائية كما ذكرنا اولاً التفاعلات الطاردة للحرارة وهى تحدث بشكل تلقائى وتبعث الحرارة كأحد صور الطاقة الناتجه عنها.
- وتعد هذا النوع من التفاعلات يعل على زيادة نسبة الانتروبيا فى النظام حيث تسبب فقدان الحرارة فى الاماكن المحيطة بها.
- كما تؤدى الى انخفاض محتوى الحرارة فى المختبر والتى تنتج عن التفاعلات الباعثه للحرارة والتى تسبب احياناً الانفجار.
- أما عن النوع الاخر من التفاعلات وهى التفاعلات الماصة للحرارة وهى تقوم بمص بمص الطاقة من أجل إكمال التفاعل.
- وفى هذا النوع من التفاعلات يجب أن يتم العمل كى تحدث اذ انها لا تحدث بشكل تلقائى مثل التفاعلات الباعثة للحرارة.
- لذا عند اجراء هذا التفاعل الماص للحرارة فإن يتم فيها قياس انخفاض درجة الحرارة اثناء اجراء التفاعل.
- ويتميز هذا النوع من التفاعلات الماصة للحرارة او التفاعلات الداخليه بأنها تعمل على زيادة المحتوى الحرارى وتدفق حرارى موجب التفاعل.
اقرا ايضا
امثلة على تفاعلات ماصة وطاردة للحرارة
اولاً مثال على تفاعل ماص للحرارة
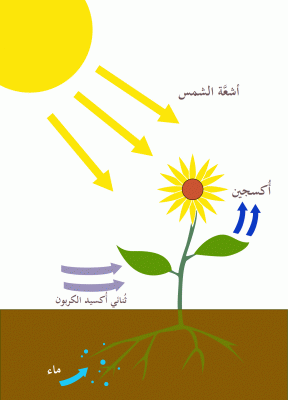
- ويعد التمثيل الضوئى هو أوضح الامثله لعمليه التفاعلات الماصة للحرارة حيث تعمل فية النباتات على امتصاص الطاقة الحراري من الشمس.
- واخراجها على هيئة ثانى اكسيد الكربون لذا فإن فى هذه العملية تقوم النباتات باستخدام الطاقة من الشمس كى تحولها لثانى اكسيد الكربون.
- كما تحول الماء فيها الى الجلوكوز والاكسجين ولكى يحدث هذا التفاعل فإنه يتطلب حوالى 15 ميجا جول من الطاقة والتى تتمثل فى ضوء الشمس.
- أى أنها تحتاج 15 ميجا جول لكل كيلو جرام من الجلوكوز الذى يتم إنتاجه من الماء فى عملية التمثيل الضوئى للنباتات.
- ويشرح هذا التفاعل المعادلة الاتية: 6CO2 + 12H2O + Light Energy → C6H12O6 + 6O2 + 6H2O
ثانياً مثال على تفاعل طارد للحرارة

- وفى علم الكيمياء فإن التفاعلات الطاردة للحرارة هى تفاعلات ينتج عنها الحرارة والتى قد تحول نتيجة امتصاص الطاقة.
- ويوجد العديد من الامثلة التى توضح كيفية عمل التفاعلات الطاردة للحرارة مثل احتراق الخشب.
- ففى هذا المثال البسيط يحدث أن يتم اتحاد الكربون مع الاكسجين وينتج عن اتحادهما انبعاث الحرارة فى المادة والتى تعبر عنها فى هذه الحالة هو الخشب.
- لذا يمكن توضيح هعملية التفاعل هذه فى هذه المعادلة البسيطة: المتفاعلات ← النواتج + طاقة.
- ويوجد العديد من الامثلة ايضاً التى توضح العمليات الباعثة للحرارة او الطاردة للحرارة حيث يعبر عنها تفاعل الترمايت.
- ويتم هذا التفاعل على سبيل المثال من خلال خلط حمض وانشاء قاعدة لتشكيل الملح والماء.
- كما يعبر عن تفاعلات الطاردة للحرارة معظم التفاعلات التى تحدث فى عملية البلمرة بالاضافة الى صور احتراق الوقود.
- كما يعبر عنه الانشطار النووى وتأكل المعادن والتى تحدث نتيجة تعرضها للأكسدة.
- كما أن عملية تحليل الحمض فى الماء عبارة عن تفاعل طارد للحرارة.
